Molecuultheorie en temperatuur
 De molecuultheorie is een belangrijke theorie in de natuur- en scheikunde. De molecuultheorie heeft onze kijk op stoffen enorm veranderd. De kennis die de theorie ons brengt stelt ons in staat meer te snappen over de verschillende fasen waarin een stof zich kan bevinden en de temperatuur die daar bij hoort.
De molecuultheorie is een belangrijke theorie in de natuur- en scheikunde. De molecuultheorie heeft onze kijk op stoffen enorm veranderd. De kennis die de theorie ons brengt stelt ons in staat meer te snappen over de verschillende fasen waarin een stof zich kan bevinden en de temperatuur die daar bij hoort.Basis
Sta je onder de douche dan zal een klein deel van het warme douchewater verdampen. Hierdoor wordt in de loop van de tijd de lucht in de badkamer steeds vochtiger. Als die warme, vochtige lucht in de buurt komt van een koeler oppervlak dan vormen zich kleine druppeltjes. De waterdamp condenseert dan. Er is warmte nodig om een vloeistof te laten verdampen. Je merkt dat goed als je een druppel van een geurstof op je huid aanbrengt. De alcohol daarin verdampt snel en koelt je wang daardoor af. Om dit verschijnsel te verklaren is het nodig de molecuultheorie te kennen. De molecuultheorie wordt hieronder beschreven.Molecuultheorie
Allerlei eigenschappen van stoffen kunnen we verklaren met de molecuultheorie. Belangrijke punten uit de theorie zijn:- Stoffen zijn opgebouwd uit hele kleine deeltjes, die we moleculen noemen
- Moleculen bestaan uit nog kleinere deeltjes, die we atomen noemen
- Tussen moleculen werken zwakke aantrekkingskrachten; de vanderwaalskrachten
- Hoe groter de afstand tussen twee moleculen, hoe kleiner de vanderwaalskracht
- Tussen moleculen zit intermoleculaire ruimte
- Moleculen zijn constant in beweging en komen daarbij met elkaar in botsing
Alle stoffen zijn chemisch gezien in drie groepen te verdelen:
- Zouten
- Metalen
- Moleculaire stoffen
De molecuultheorie als geheel kun je alleen maar gebruiken voor moleculaire stoffen. Voor zouten en metalen is de theorie slechts gedeeltelijk te gebruiken. Zo is in zouten de aantrekkingskracht tussen de ionen veel sterker dan de vanderwaalskracht.
De fasen van een stof
De meeste stoffen kunnen in drie verschillende fasen voorkomen:- De vaste fase
- De vloeibare fase
- De gasvormige fase
In de vaste- en vloeibare fase zitten de moleculen dicht opeen, in verhouding tot hun afmeting. Moleculen trekken elkaar aan door cohesie: krachten tussen moleculen van dezelfde soort, of adhesie: krachten tussen moleculen van verschillende soort. Het verschil tussen de vaste- en de vloeibare fase is dat bij vaste stoffen de moleculen om een evenwichtsstand trillen maar op hun plaats blijven gebonden, terwijl bij vloeistoffen de moleculen vrij door elkaar kunnen bewegen.
In de gasvormige fase zitten de moleculen, relatief, ver uit elkaar en trekken elkaar niet merkbaar aan. Ook kunnen ze, net als in de vloeibare fase, vrij door elkaar bewegen.
 Bron: Sawims, Wikimedia Commons (Publiek domein)
Bron: Sawims, Wikimedia Commons (Publiek domein)Faseovergangen
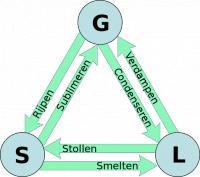
Het veranderen van de ene fase in de andere fase wordt een faseovergang genoemd. Elke faseovergang heeft een bepaalde naam. Op de afbeelding hiernaast staat de S voor de vaste fase (solid), en de L voor de vloeibare fase (liquid).Hieronder de faseovergangen beschreven:
- Van vast naar vloeibaar is smelten
- Van vloeibaar naar vast is stollen
- Van vloeibaar naar gasvormig is verdampen
- Van gasvormig naar vloeibaar is condenseren
- Van gasvormig naar vast is rijpen
- Van vast naar gasvormig is sublimeren
Niet alle stoffen kunnen in drie fasen voorkomen. Er bestaan vaste stoffen die bij verwarming niet smelten en verdampen, maar ontleden. Deze stoffen heten thermoharders. Door de vertakte structuur van koolstofketens is de stof te 'sterk' om te smelten.
Temperatuur
Moleculen en ionen zijn voortdurend in beweging en hebben daardoor kinetische energie. Bij constante temperatuur verandert de gemiddelde kinetische energie van deze deeltjes niet. Bij een temperatuurstijging neemt de gemiddelde kinetische energie toe en bij een temperatuurdaling neemt deze af. De temperatuur is dus een maat voor de gemiddelde kinetische energie van moleculen. De temperatuur daalt dus als de kinetische energie van de moleculen afneemt. De temperatuur kan niet verder dalen als de moleculen geen kinetische energie meer hebben, dus als de moleculen niet meer bewegen. Voor alle moleculen is dat het geval bij een temperatuur van -273,15 graden Celsius. Deze laagste temperatuur wordt het absolute nulpunt genoemd.Het bestaan van een absoluut nulpunt heeft geleid tot de invoering van een nieuwe temperatuurschaal. Deze schaal begint bij het absolute nulpunt en heeft een verdeling in Kelvin (K). Een stijging van 1 K is gelijk aan een stijging van 1 graden Celsius.
Een formule voor het verband tussen Kelvin (K) en Celsius (C) is dus: K=C+273,15